Cellulaire geheimen van veroudering ontgrendeld door onderzoekers
Datum: 1 juni 2022
Bron: Wellcome Trust Sanger
Samenvatting van het instituut: Onderzoekers hebben ontdekt hoe genetische mutaties die zich gedurende een mensenleven langzaam ophopen, leiden tot dramatische veranderingen in de manier waarop bloed wordt gevormd na de leeftijd van 70 jaar, wat een nieuwe theorie voor veroudering oplevert.
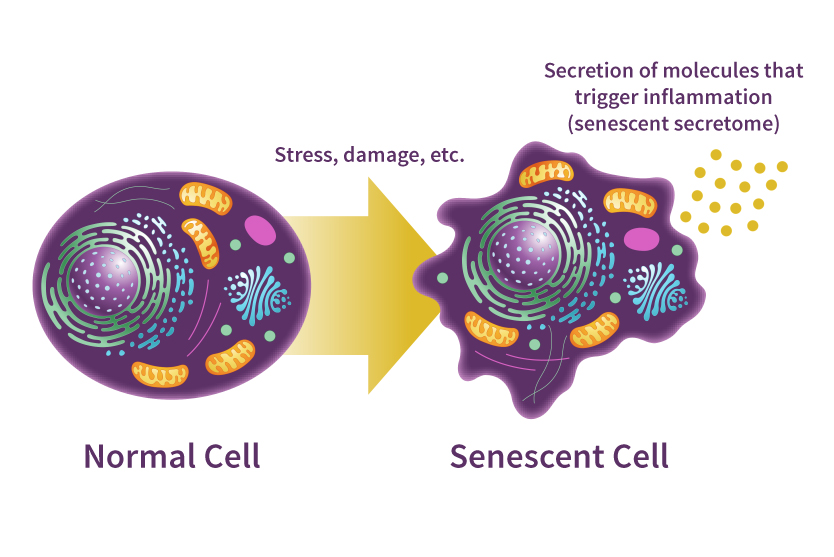
Cellulaire senescentie – veroudering ontgrendeld:
Nieuw onderzoek heeft aangetoond hoe genetische veranderingen die zich gedurende het hele leven langzaam ophopen in bloedstamcellen, waarschijnlijk verantwoordelijk zijn voor de dramatische verandering in de bloedproductie na de leeftijd van 70 jaar.
De studie, door wetenschappers van het Wellcome Sanger Institute, het Wellcome-MRC Cambridge Stem Cell Institute en medewerkers, is vandaag (1 juni) gepubliceerd in het tijdschrift NATUUR, en suggereert een nieuwe theorie van veroudering.
Alle menselijke cellen krijgen gedurende het hele leven genetische veranderingen, bekend als somatische mutaties. Veroudering wordt waarschijnlijk veroorzaakt door de accumulatie van meerdere soorten schade aan onze cellen in de loop van de tijd, waarbij één theorie is dat de opbouw van somatische mutaties ervoor zorgt dat cellen geleidelijk aan functionele reserve verliezen. Het is echter momenteel onduidelijk hoe een dergelijke geleidelijke opeenhoping van moleculaire schade zich zou kunnen vertalen in de abrupte verslechtering van het functioneren van onze organen na de leeftijd van 70 jaar.
Om dit verouderingsproces te onderzoeken, heeft het team van het Wellcome Sanger Institute, de Cambridge Stamcelinstituut en medewerkers bestudeerden de productie van bloedcellen uit het beenmerg en analyseerden 10 personen in leeftijd variërend van pasgeborenen tot ouderen. Ze hebben de hele genomen van 3,579 bloedstamcellen gesequenced en alle somatische mutaties in elke cel geïdentificeerd. Het team gebruikte dit om 'stambomen' van de bloedstamcellen van elke persoon te reconstrueren, en liet voor het eerst een onbevooroordeeld beeld zien van de relaties tussen bloedcellen en hoe deze relaties veranderen gedurende de menselijke levensduur.
De onderzoekers ontdekten dat deze 'stambomen' drastisch veranderden na de leeftijd van 70 jaar. De productie van bloedcellen bij volwassenen onder de 65 jaar bedroeg 20,000 tot 200,000 stamcellen, die elk in ongeveer gelijke hoeveelheden bijdroegen. Daarentegen was de bloedproductie bij personen ouder dan 70 jaar zeer ongelijk. Een verminderde set van geëxpandeerde stamcelklonen - slechts 10 tot 20 - droeg bij tot de helft van alle bloedproductie bij elke onderzochte oudere persoon. Deze zeer actieve stamcellen waren gedurende het leven van die persoon geleidelijk in aantal toegenomen, veroorzaakt door een zeldzame subset van somatische mutaties die bekend staat als 'driver-mutaties'.
Deze bevindingen brachten het team ertoe een model voor te stellen waarin leeftijdsgebonden veranderingen in de bloedproductie het gevolg zijn van somatische mutaties die ervoor zorgen dat 'egoïstische' stamcellen het beenmerg bij ouderen domineren. Dit model, met de gestage introductie van driver-mutaties die de groei van functioneel veranderde klonen gedurende tientallen jaren veroorzaken, verklaart de dramatische en onvermijdelijke verschuiving naar een verminderde diversiteit van bloedcelpopulaties na de leeftijd van 70 jaar. Welke klonen dominant worden, verschilt van persoon tot persoon, en dus verklaart het model ook de variatie die wordt waargenomen in ziekterisico en andere kenmerken bij oudere volwassenen. Een tweede studie, ook vandaag gepubliceerd in NATUUR, onderzoekt hoe verschillende individuele drivermutaties de celgroeisnelheid in de loop van de tijd beïnvloeden.
Dr. Emily Mitchell, hematologieregistrar bij Addenbrooke's Hospital, PhD-student bij het Wellcome Sanger Institute, en hoofdonderzoeker van de studie, zei: "Onze bevindingen tonen aan dat de diversiteit van bloedstamcellen op oudere leeftijd verloren gaat als gevolg van positieve selectie van sneller groeiende klonen met drivermutaties. Deze klonen 'concurreren' de langzamer groeiende klonen. In veel gevallen brengt deze verhoogde fitheid op stamcelniveau waarschijnlijk een prijs met zich mee - hun vermogen om functionele rijpe bloedcellen te produceren is aangetast, wat het waargenomen leeftijdsgerelateerde functieverlies in het bloedsysteem verklaart."
Dr. Elisa Laurenti, assistent-professor en Wellcome Royal Society Sir Henry Dale Fellow aan het Wellcome-MRC Cambridge Stem Cell Institute aan de Universiteit van Cambridge, en mede-senior onderzoeker van deze studie, zei: "Factoren zoals chronische ontsteking, roken, infectie en chemotherapie veroorzaken eerdere groei van klonen met kankerverwekkende mutaties. We voorspellen dat deze factoren ook de afname van de diversiteit van de bloedstamcellen in verband met veroudering naar voren brengen. Het is mogelijk dat er factoren zijn die dit proces ook kunnen vertragen. We hebben nu de spannende taak om uit te zoeken hoe deze nieuw ontdekte mutaties de bloedfunctie bij ouderen beïnvloeden, zodat we kunnen leren hoe we het ziekterisico kunnen minimaliseren en gezond ouder worden kunnen bevorderen.”
Dr. Peter Campbell, hoofd van het Cancer, Aging and Somatic Mutation Program aan het Wellcome Sanger Institute, en senior onderzoeker van de studie, zei: "We hebben voor de eerste keer aangetoond hoe gestaag accumulerende mutaties gedurende het hele leven leiden tot een catastrofale en onvermijdelijke verandering in bloedcelpopulaties na de leeftijd van 70 jaar. Wat super opwindend is aan dit model is dat het ook in andere orgaansystemen kan worden toegepast. We zien dat deze egoïstische klonen met drivermutaties zich uitbreiden met de leeftijd in veel andere weefsels van het lichaam - we weten dat dit het risico op kanker kan verhogen, maar het kan ook bijdragen aan andere functionele veranderingen die verband houden met veroudering."
Dit onderzoek werd gefinancierd door Wellcom en de William B Harrison Foundation.
Verhaal Bron:
Materialen door Welkom Trust Sanger Institute. Opmerking: inhoud kan worden bewerkt voor stijl en lengte.
Journal Reference:
- Emily Mitchell, Michael Spencer Chapman, Nicholas Williams, Kevin J. Dawson, Nicole Mende, Emily F. Calderbank, Hyunchul Jung, Thomas Mitchell, Tim HH Coorens, David H. Spencer, Heather Machado, Henry Lee-Six, Megan Davies, Daniel Hayler, Margarete A. Fabre, Krishnaa Mahbubani, Federico Abascal, Alex Cagan, George S. Vassiliou, Joanna Baxter, Inigo Martincorena, Michael R. Stratton, David G. Kent, Krishna Chatterjee, Kourosh Saeb Parsy, Anthony R. Green, Jyoti Nangalia, Elisa Laurenti & Peter J. Campbell. Klonale dynamiek van hematopoëse gedurende de menselijke levensduur. NATUUR, 2022 DOI: 10.1038 / s41586-022-04786-y






